Goutte
| Goutte | |
|---|---|
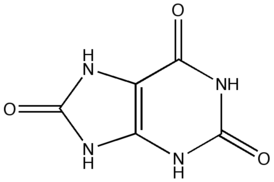 acide urique | |
| ICD-10 | M Dix. |
| ICD-10-KM | et |
| ICD-9 | 274,0 274.1 274,8 274,9 |
| ICD-9-KM | , , et |
| OMIM | 138900 |
| Diseasesdb | 29031 |
| Medlineplus | |
| eMedicine | émergent / 221 med / 924 med / 1112 oph / 506 orthopédique / 124 radio / 313 |
| Engrener | D006073 |
Goutte ( . Grec ancien ποδάγρα , littéralement - jambe piège ; de πούς , genre n .. Ποδός - pied et ἄγρα - pêche, chasse ) [3] - maladie métabolique caractérisée par le dépôt dans divers tissus du corps de cristaux d'urate sous forme de monourate de sodium ou acide urique . L'occurrence est basée sur l'accumulation d'acide urique et une diminution de son excrétion par les reins , ce qui conduit à une augmentation de la concentration de l'acide urique dans le sang ( hyperuricémie) Cliniquement, la goutte se manifeste par une arthrite aiguë récurrente et la formation de ganglions goutteux - tofus . Les lésions rénales sont également l'une des principales manifestations cliniques de la goutte avec l'arthrite. Le plus souvent, la maladie survient chez les hommes, mais récemment, la prévalence de la maladie chez les femmes a augmenté, avec l'âge, la prévalence de la goutte augmente. Pour le traitement, des médicaments qui affectent le mécanisme pathogénique de la maladie sont utilisés , ainsi que des médicaments pour le traitement symptomatique.
Histoire
La goutte est connue depuis l'antiquité. La première preuve documentée de la maladie est connue de l'Égypte ancienne et remonte à 2600 av. e. [4] Ils sont basés sur une description de l'arthrite goutteuse du pouce [4] . Le guérisseur et docteur grec ancien Hippocrate au V siècle av. e. a décrit les symptômes cliniques de l'arthrite goutteuse dans ses «Aphorismes», où il a noté que la maladie ne se manifestait pas chez les eunuques et les femmes jusqu'à la ménopause [5] [6] . Le philosophe et médecin romain Aulus Cornelius Celsus a décrit la relation entre le développement de la goutte et la consommation d'alcool et l'insuffisance rénale associée [7]. En 150, Galen a souligné que la goutte était causée par «la licence, l'incontinence et l'hérédité» [8] .
À la fin du XVIIe siècle, le clinicien anglais Thomas Sydenham , qui souffrait de goutte depuis plus de 30 ans, la classa comme une maladie distincte et décrivait très précisément le tableau clinique d'une crise aiguë d'arthrite goutteuse dans le Traité de la goutte ( latin: Tractatus de podagra et hydrope ) . Il y compare le syndrome douloureux de la goutte à la douleur «due à la pression des membres» et décrit les sensations du patient, comparables à la façon dont «un énorme chien creusait le doigt avec des crocs» [9] . En 1679, le scientifique néerlandais Anthony van Levenguk a décrit pour la première fois la structure microscopique des cristaux d'acide urique [5] .
En 1848, le physiologiste anglais Alfred Baring Garrod (1819-1906), utilisant un fil trempé dans le sang d'un patient souffrant de goutte, découvre et décrit le fait d'une augmentation de l'acide urique dans le sang avec cette maladie [10] [11] [12 ] ] .
Les premiers travaux scientifiques du médecin français Jean Martin Charcot comprennent la goutte: « dégâts Cartilage due à la goutte » ( français Les altérations des cartilages Dans la gouite , 1858), des « dépôts goutteux (de tofus) dans l'oreille externe de la goutte » ( Les concrétions tophacées de l'oreille externe chez les goutteux , 1860), «Changements dans les reins avec la goutte» ( Les altérations du rein chez les goutteux , 1864), «Sur la goutte et l'empoisonnement au plomb» ( Les rapports de la goutte et de l'intoxication saturnine , 1864).
En 1899, la présence de cristaux d'urate dans le liquide articulaire a été découverte lors d'une crise d'arthrite goutteuse. En 1961, MacCarty et Hollander ont révélé le rôle des cristaux d'urate dans l'apparition et le développement de l'inflammation goutteuse [13] .
Historiquement, du Moyen-Âge au XXe siècle, la plupart des riches et des nobles souffraient de goutte, à propos de laquelle on l'appelait «la maladie des rois» [4] [14] , «la maladie des riches» et «la maladie des aristocrates» [4] . On pensait qu'elle était associée à un excès de poids, une suralimentation (en particulier l'abus de viande) et une consommation excessive de boissons alcoolisées. Par exemple, en 1739, le Français Eugène Mushron ( fr. Eugène Moucheron) a publié une brochure intitulée «On Noble Gout and its Accompagning Vertues», dans laquelle il a salué la goutte et a noté qu'il s'agissait d'une maladie des rois, des princes, des chefs militaires éminents, des personnes intelligentes et douées, et a également cité des exemples de personnes couronnées, de politiciens et d'artistes, souffrant de goutte [15] . Un nouvel élan d'intérêt pour la goutte est apparu au début du 20e siècle, lorsque Havelock Ellis ( Eng. Henry Havelock Ellis , 1859-1939) a publié en 1927 un livre intitulé The History of English Genius. L'auteur y traite du sujet de la goutte et cite comme exemple 55 éminents anglais bien connus qui en souffrent [16] . En 1955, l'œuvre d' Egon Orowan , L'Origine de l'homme , publiée dans la revueNature », dans lequel il a décrit l'augmentation de l'incidence des infections de goutte chez les génies et a expliqué que l'acide urique est structurellement très similaire aux purines méthylées: la caféine , la théophylline et la théobromine , qui sont des stimulants de l'activité mentale qui ont un effet stimulant sur les fonctions cérébrales supérieures, en particulier , durée d'attention et capacité de concentration. Orovan a souligné que l'acide urique chez tous les mammifères développés , à l'exception des singes anthropoïdes et des humains, est décomposé par l'action de l'enzyme uricase produite dans le foie en allantoïne, chez les primates, en raison du manque d'uricase, il reste dans le sang [16]
Épidémiologie
L'hyperuricémie est détectée dans 4 à 12% de la population, 0,1% de la population russe souffre de goutte [17] . Aux États-Unis et en Europe, 2% des personnes souffrent de goutte, chez les hommes âgés de 55 à 65 ans, 4 à 6% souffrent de goutte.
Le rapport hommes / femmes est compris entre 7: 1 et 19: 1. L'incidence maximale se produit dans 40-50 ans chez les hommes, 60 ans et plus chez les femmes. Avant la ménopause, les femmes tombent rarement malades, probablement en raison de l'effet des œstrogènes sur l'excrétion d'acide urique [17] .
La fréquence de l'arthrite goutteuse dans différentes populations varie de 5 à 50 pour 1000 hommes et de 1 à 9 pour 1000 femmes, et le nombre de nouveaux cas par an est de 1 à 3 pour 1000 chez les hommes et de 0,2 pour 1000 chez les femmes [17] . Au cours de la dernière décennie[ quand? ] l' incidence de la goutte a augmenté [18] .
Une crise aiguë de goutte chez l'adolescent et le jeune est rarement observée, elle est généralement médiée par un défaut primaire ou secondaire dans la synthèse de l'acide urique [17] .
Étiologie
Facteurs de développement de la maladie
Il existe un certain nombre de facteurs de risque qui contribuent à l'apparition et au développement de la goutte chez certaines personnes.
Les facteurs de risque de goutte comprennent l' hypertension artérielle , l' hyperlipidémie et également:
- augmentation de l'apport de bases puriques dans le corps , par exemple, lors de la consommation d'une grande quantité de viande rouge (en particulier les abats), certaines variétés de poisson, cacao, thé, chocolat, pois, lentilles, fructose, alcool (en particulier la bière, qui contient beaucoup de guanosine et de xanthine - précurseurs de l'acide urique );
- une augmentation du nombre de nucléotides puriques avec catabolisme général (par exemple, avec un traitement antitumoral; apoptose massive chez les personnes atteintes de maladies auto-immunes);
- inhibition de l'excrétion d'acide urique dans l'urine (par exemple, avec insuffisance rénale);
- augmentation de la synthèse d'acide urique tout en réduisant son excrétion du corps (par exemple, avec abus d'alcool, états de choc, glycogenèse avec déficit en glucose-6-phosphatase);
- prédisposition héréditaire (la nature de l'hérédité n'est pas encore complètement clarifiée).
Pathogenèse
La pathogenèse de la maladie est basée sur une augmentation du niveau d'acide urique dans le sang. Mais ce symptôme n'est pas synonyme de la maladie, car une hyperuricémie est également observée avec d'autres maladies (maladies du sang, tumeurs, maladies rénales, etc.), une surcharge physique extrêmement élevée et la consommation d'aliments gras.
Il existe au moins trois éléments principaux de l'apparition de la goutte:
- accumulation de composés d'acide urique dans le corps;
- dépôt de ces composés dans les organes et les tissus;
- le développement d'attaques aiguës d'inflammation dans ces lésions, la formation de granulomes goutteux et de "cônes" goutteux - des tofus, généralement autour des articulations.
Symptômes et évolution de la maladie
L'évolution naturelle complète de la goutte passe par quatre étapes:
- hyperuricémie asymptomatique;
- arthrite goutteuse aiguë ;
- période intercritique;
- dépôts goutteux chroniques dans les articulations.
La néphrolithiase peut se développer à n'importe quel stade sauf le premier. Il y a une concentration constamment accrue d'acide urique dans le plasma sanguin et dans l'urine; inflammation articulaire du type de la monoarthrite, qui s'accompagne de fortes douleurs et de fièvre; urolithiase et pyélonéphrite récurrente, entraînant une néphrosclérose et une insuffisance rénale.
Diagnostics
Le diagnostic de l'arthrite goutteuse peut être posé sur la base des critères diagnostiques épidémiologiques adoptés lors du troisième symposium international sur l'étude des maladies rhumatismales, New York , 1966 .
1. Avec détection chimique ou microscopique de cristaux d'acide urique dans le liquide synovial ou dépôt d'urates dans les tissus.
2. S'il existe deux ou plusieurs de ces critères:
- une histoire claire et / ou une observation d'au moins deux crises de douleur, un gonflement des articulations des extrémités (les crises, au moins aux premiers stades, devraient commencer soudainement par une douleur intense; une rémission clinique complète devrait se produire dans les 1-2 semaines );
- une histoire claire et / ou l'observation d'une crise de goutte (voir ci-dessus) avec des dommages au gros orteil;
- tofus cliniquement prouvé; une histoire claire et / ou l'observation d'une réaction rapide à la colchicine , c'est-à-dire une diminution des signes objectifs d'inflammation dans les 48 heures après le début du traitement.
Une étude aux rayons X n'est pas incluse dans la liste des tests de diagnostic requis, mais elle peut montrer des dépôts de cristaux de tofus et des dommages au tissu osseux à la suite d'inflammations répétées. Une radiographie peut également être utile pour surveiller les effets de la goutte chronique sur les articulations.
La détection de l'hyperuricémie ne suffit pas pour établir un diagnostic, puisque seulement 10% des personnes atteintes d'hyperuricémie souffrent de goutte [17] .
Critères diagnostiques de la goutte (OMS 2000)
I. La présence d'urates cristallins caractéristiques dans le liquide articulaire.
II. La présence de tofus (prouvés) contenant des urates cristallins, confirmée chimiquement ou par microscopie à polarisation.
III. La présence d'au moins 6 des 12 signes ci-dessous:
- plus d'une histoire aiguë de crise d'arthrite;
- inflammation maximale de l'articulation le premier jour;
- nature monoarticulaire de l'arthrite;
- hyperémie de la peau sur l'articulation touchée;
- gonflement ou douleur localisée dans l'articulation métatarso-phalangienne;
- dommages unilatéraux aux articulations de la voûte plantaire;
- formations nodulaires ressemblant à des tofus ;
- hyperuricémie
- lésion unilatérale de l'articulation métatarso-phalangienne;
- gonflement asymétrique de l'articulation touchée;
- détection sur radiographie de kystes sous-corticaux sans érosion;
- absence de flore dans le liquide articulaire.
Les signes les plus fiables sont l'arthrite aiguë ou, moins fréquemment, subaiguë, la détection d'urates cristallins dans le liquide synovial et la présence de tofus éprouvés. Les cristaux d'urate ressemblent à des bâtons ou à de fines aiguilles aux extrémités cassées ou arrondies d'environ 10 microns de long. Les microcristaux d' urates dans le liquide synovial se trouvent à la fois librement couchés et dans les neutrophiles .
Diagnostics différentiels
La goutte se différencie par la septicémie , qui peut survenir parallèlement à celle-ci, ainsi que par d'autres arthrites microcristallines (synovite cristalline, principalement avec chondrocalcinose (principalement avec dépôt de pyrophosphate de calcium - en particulier chez les personnes âgées); polyarthrite réactive , psoriasique et rhumatoïde .
Traitement
Les patients atteints de goutte, d'abord détectés ou lors d'une exacerbation de la maladie, sont soumis à un traitement hospitalier dans les services de rhumatologie spécialisés des hôpitaux régionaux ou municipaux. Les patients atteints de goutte pendant la période de rémission de la maladie, à condition qu'un traitement adéquat soit prescrit, peuvent être supervisés par un rhumatologue , néphrologue au lieu de résidence dans les cliniques de district. La durée approximative du traitement dans des conditions stationnaires (services de rhumatologie spécialisés) est de 7 à 14 jours, sous réserve de la sélection d'une thérapie efficace adéquate, de l'amélioration des signes cliniques et biologiques de la maladie.
À ce jour, la pharmacologie moderne n'a pas été en mesure de présenter un seul médicament qui serait à la fois universel et pourrait vraiment résoudre le problème du traitement de la goutte.
Le traitement de la goutte implique:
- si possible, un soulagement rapide et soigneux d'une crise aiguë;
- prévention de la rechute de l'arthrite goutteuse aiguë;
- la prévention ou la régression des complications de la maladie causées par le dépôt de cristaux d'urate de sodium monosubstitué dans les articulations, les reins et d'autres tissus;
- la prévention ou la régression de symptômes concomitants tels que l' obésité , l' hypertriglycéridémie ou l' hypertension ;
- prévention de la formation de calculs rénaux d'acide urique.
Traitement pour une crise aiguë de goutte
Dans l'arthrite goutteuse aiguë, un traitement anti-inflammatoire est effectué. Le plus souvent utilisé colchicine. Il est prescrit pour une administration par voie orale, généralement à une dose de 0,5 mg toutes les heures ou 1 mg toutes les 2 heures, et le traitement est poursuivi jusqu'à ce que: 1) il y ait un soulagement de l'état du patient; 2) il n'y aura pas d'effets indésirables du tractus gastro-intestinal ou 3) la dose totale du médicament n'atteindra pas 6 mg dans le contexte sans effet. La colchicine est plus efficace si le traitement est commencé peu de temps après l'apparition des symptômes. Au cours des 12 premières heures de traitement, la condition s'améliore considérablement chez plus de 75% des patients. Cependant, chez 80% des patients, le médicament provoque des effets indésirables du tractus gastro-intestinal, qui peuvent survenir plus tôt ou simultanément avec une amélioration clinique. Lorsqu'il est ingéré, le niveau maximal de colchicine dans le plasma est atteint après environ 2 heures. Par conséquent, nous pouvons supposer que son apport est de 1,0 mg toutes les 2 heures est moins susceptible de provoquer l'accumulation d'une dose toxique jusqu'à ce qu'un effet thérapeutique se produise. Cependant, étant donné que l'effet thérapeutique est associé au niveau de colchicine dans les leucocytes et non dans le plasma, l'efficacité du schéma thérapeutique nécessite une évaluation plus approfondie.
Avec l'administration intraveineuse de colchicine, les effets secondaires du tractus gastro-intestinal ne se produisent pas et l'état du patient s'améliore plus rapidement. Après une seule injection, le niveau du médicament dans les leucocytes augmente, restant constant pendant 24 heures, et peut être déterminé même après 10 jours. En tant que dose initiale, 2 mg doivent être administrés par voie intraveineuse, puis, si nécessaire, répéter l'administration de 1 mg deux fois avec un intervalle de 6 heures.Des précautions particulières doivent être prises avec l'administration de colchicine. Elle est irritante et, si elle pénètre dans les tissus environnants, peut provoquer de graves douleurs et nécroses.. Il est important de se rappeler que la voie d'administration intraveineuse nécessite une précision et que le médicament doit être dilué dans 5 à 10 volumes de solution saline normale, et la perfusion doit être poursuivie pendant au moins 5 minutes. Avec une administration orale et parentérale, la colchicine peut inhiber la fonction de la moelle osseuse et provoquer une alopécie, une insuffisance cellulaire hépatique, une dépression mentale, des convulsions, une paralysie ascendante, une dépression respiratoire et la mort. Les effets toxiques sont plus probables chez les patients présentant une pathologie du foie, de la moelle osseuse ou des reins, ainsi que ceux recevant des doses d'entretien de colchicine. Dans tous les cas, la dose doit être réduite. Il ne doit pas être prescrit aux patients atteints de neutropénie.
Dans l'arthrite goutteuse aiguë, d'autres médicaments anti-inflammatoires sont également efficaces, notamment l' indométacine , la phénylbutazone , le naproxène , l'étoricoxib, etc.
L'indométacine peut être prescrite pour une administration orale à une dose de 75 mg, après quoi toutes les 6 heures le patient doit recevoir 50 mg; le traitement avec ces doses se poursuit le lendemain de la disparition des symptômes, puis la dose est réduite à 50 mg toutes les 8 heures (trois fois) et à 25 mg toutes les 8 heures (également trois fois). Les effets secondaires de l'indométacine comprennent des troubles gastro-intestinaux, une rétention de sodium et des symptômes du système nerveux central. Malgré le fait que ces doses peuvent provoquer des effets secondaires chez près de 60% des patients, l'indométacine est généralement plus facilement tolérée que la colchicine et est probablement le traitement de choix pour l'arthrite goutteuse aiguë. Médicaments d'excrétion d'acide urique et allopurinolavec une crise aiguë, la goutte est inefficace. Dans la goutte aiguë, en particulier avec des contre-indications ou l'inefficacité de la colchicine et des anti-inflammatoires non stéroïdiens, l'administration systémique ou locale (c'est-à-dire intra-articulaire) de glucocorticoïdes est bénéfique. Pour une administration systémique, qu'elle soit orale ou intraveineuse, des doses modérées doivent être prescrites pendant plusieurs jours, car la concentration de glucocorticoïdes diminue rapidement et leur action cesse. L'administration intra-articulaire d'un stéroïde à action prolongée (par exemple , l'hexacétonide de triamcinolone à une dose de 15 à 30 mg) peut arrêter une crise de monoarthrite ou de bursite en 24 à 36 heures. Ce traitement est particulièrement recommandé s'il n'est pas possible d'utiliser un schéma posologique standard.
Régime
Les directives diététiques traditionnelles sont de limiter votre consommation de purines et d'alcool. Les aliments riches en purines comprennent les produits à base de viande et de poisson, ainsi que le thé, le cacao et le café. Récemment, il a également été démontré que la perte de poids due à une restriction modérée des glucides et des aliments riches en calories, combinée à une augmentation proportionnelle des protéines et des acides gras insaturés, chez les patients souffrant de goutte, entraînait une diminution significative des niveaux d'acide urique et une dyslipidémie [19] .
Voir aussi
- Arthrite microcristalline
- Chondrocalcinose
- Urata
- Acide urique
- Tofus
Notes
- ↑ Retourner: 1 2 3 4 Monarch Disease Ontology version 2018-06-29sonu- 2018-06-29 - 2018.
- ↑ Retourner: 1 2 3 4 Disease Ontology release 2019-05-13- 2019-05-13 - 2019.
- ↑ Gout / V. G. Barskov // Pérou - Semi-remorque. - M .: Great Russian Encyclopedia, 2014. - P. 524. - ( Great Russian Encyclopedia : [en 35 volumes.] / Ch. Ed. Yu. S. Osipov ; 2004—2017, vol. 26). - ISBN 978-5-85270-363-7 .
- ↑ Retourner: 1 2 3 4 Richette P., Bardin T.Gout // Lancet. - Janvier 2010. - Vol. 375,n ° 9711. - P. 318—328. -doi:10.1016 / S0140-6736 (09) 60883-7. -PMID 19692116.
- ↑ Retourner: 1 2 Pillinger MH, Rosenthal P., Abeles AM Hyperuricémie et goutte: nouvelles perspectives sur la pathogenèse et le traitement // Bulletin du NYU Hospital for Joint Diseases. - 2007. - Vol. 65,n ° 3. - P. 215-221. -PMID 17922673. Archivé le 16 décembre 2008.
- ↑ Les aphorismes des archives Internet Classics d'Hippocrate . MIT .
- ↑ A. Cornelius Celsus. Sur la médecine . Université de Chicago .
- ↑ Zilva J. F., Pannell P. R. Chimie clinique dans le diagnostic et le traitement. - M .: Médecine, 1988 .-- 528 p. - ISBN 5-225-00220-X .
- ↑ Nasonova V., Barskova V. Maladie de l'abondance // Science et vie . - 2004. - n ° 7 .
- ↑ Garrod AB La nature et le traitement de la goutte et de la goutte rhumatismale. - Londres: Walton et Maberly, 1859.
- ↑ Keitel W. Le grand prêtre de la goutte - Sir Alfred Baring Garrod (1819–1907) // Z Rheumatol. - 2009. - Vol. 68, n ° 10 . - P. 851-856. - doi : 10.1007 / s00393-009-0541-4 . - PMID 19937040 .
- ↑ Étage GD Alfred Baring Garrod (1819–1907) // Rhumatologie (Oxford). - 2001. - Vol. 40, n ° 10 . - P. 1189-1190. - doi : 10.1093 / rhumatologie / 40.10.1189 . - PMID 11600751 .
- ↑ McCarthy DJ, Hollander JL Identification des cristaux d'urate dans le liquide synovial goutteux. // Annales de médecine interne . - 1961. - Vol. 54. - P. 452.
- ↑ La maladie des rois - Forbes.com . Forbes .
- ↑ Zaselsky V., Lalayants I. La nature du génie // Spark . - 1996. - n ° 27 . - S. 4 .
- ↑ Retourner: 1 2 Lalayants I. L'acide urique frappe la tête. Les cônes de génie doivent être recherchés non pas sur la tête, mais sur les jambes //Autour du monde. - 2008.
- ↑ Retourner: 1 2 3 4 5 éd. S.L. Nasonova. Recommandations cliniques. Rhumatologie. - GEOTAR-Media, 2008. - P. 112-119. - 288 p. -ISBN 978-5-9704-0698-4.
- ↑ Lisa K. Stamp, Tony R. Merriman, Nicola Dalbeth. Gout (Eng.) // The Lancet. - 2016-10-22. - T. 388 , no. 10055 . - S. 2039-2052 . - ISSN 1474-547X 0140-6736, 1474-547X . - doi : 10.1016 / S0140-6736 (16) 00346-9 .
- ↑ Barskova, V.G. & Nasonova, V.A. (2002), Gout et Insulin, <http://medinfa.ru/article/31/117288/> Resistance Syndrome Archivé le 1er février 2009 sur Wayback Machine
Liens
- L'acide urique vous frappe // Dans le monde
- Maladies métaboliques
- Rhumatologie
- Maladies articulaires
More posts:
All Posts